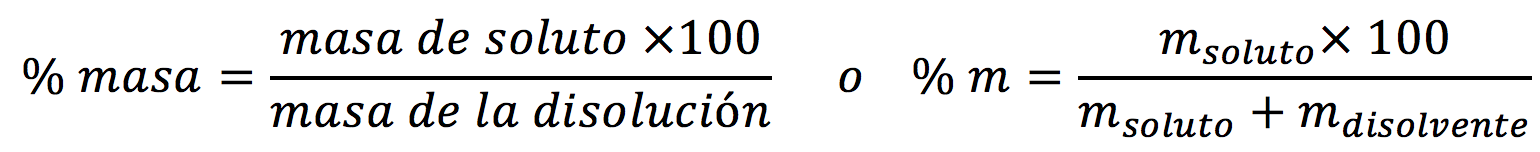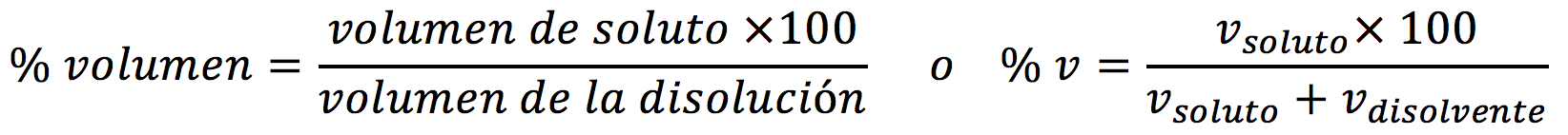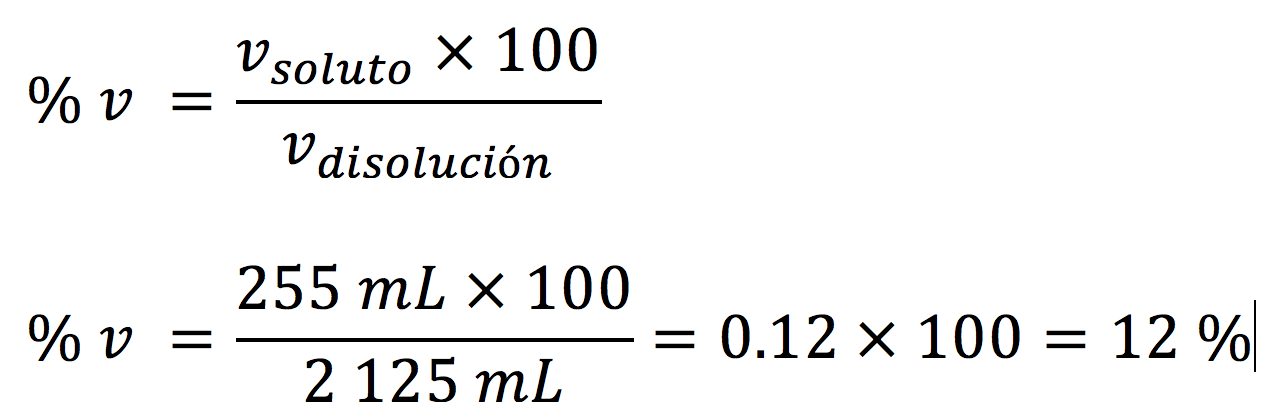Interpretación
Es importante que interpretes en el problema cuál o cómo se le llama al soluto, al disolvente y a la disolución total. A veces no mencionan alguno de ellos, pero se puede averiguar o deducir.
Para ello, fíjate en las cantidades de cada sustancia, como se muestra a continuación:
- Soluto: es la sustancia que está en menor cantidad, por lo tanto en el problema sería el azúcar.
- Disolvente: es la sustancia que está en mayor cantidad, en esta situación sería el agua.
- Disolución: es el producto final o mezcla del soluto (azúcar) con el disolvente (agua). En el problema se llamaría suero azucarado.
Te solicitan la concentración expresada en % masa, por lo que el resultado se deberá expresar en porcentaje en masa de soluto y con ello se podrá conocer los gramos de azúcar (soluto) por cada 100 gramos de suero (disolución).
Fotografía 1.1.I. Suero. Obtenida de flickr.com (CC0 1.0)
Datos
El problema nos indica la cantidad del soluto y la disolución, como sigue:
msoluto = 40 g de azúcar
mdisolvente = 180 g de agua
% m = X , esta es la incógnita o lo que se desea saber. El resultado se expresará sin unidades, pero en porcentaje (%)
¡Atención! Ya no nos preguntan nada adicional, por lo que no debes distraerte en cálculos innecesarios o en información que no sea útil.
Operaciones
Se desea saber la concentración de azúcar en el suero preparado, expresada en porcentaje masa. Para ello, tenemos la siguiente ecuación:
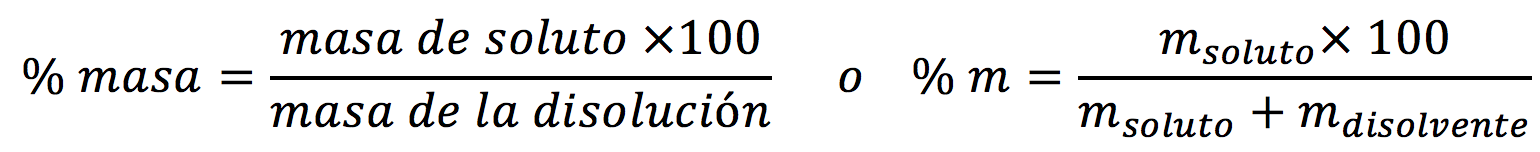
Te puedes dar cuenta que la incógnita (% m) ya está separada o despejada en el lado izquierdo de la ecuación, por lo que ya no será necesario hacer despejes adicionales. Además, tienes la información de msoluto y mdisolvente, por lo que te conviene usar la segunda forma de la ecuación (a la derecha).
Haciendo las sustituciones de los valores y las operaciones, quedaría:

Observa que las unidades gramos se cancelaron, por lo que se dice que el resultado es adimensional, pero como al final se multiplicó por un 100, entonces se expresa como porcentaje.
Resultados
El resultado obtenido fue que el suero tiene una concentración en porcentaje masa de:
% m = 18.2 % de azúcar
Esto quiere decir que por cada 100 g de suero, se tienen 18.2 g de azúcar.
Con esto ya resolvimos el problema de saber la concentración de azúcar en el suero.
Información adicional: saber resolver este tipo de problemas nos puede ayudar para conocer la proporción de azúcar en el suero si queremos para preparar cantidades mayores de esta mezcla a la misma concentración.
Por ejemplo, ¿cuánta azúcar se tendrá que adicionar si ahora se desea preparar 1 000 g de suero? Respuesta = como sabemos que debe de haber 18.2 g de azúcar por cada 100 g de suero, entonces se requerirán 182 g de azúcar para preparar 1 000 g, porque se estaría preparando 10 veces más de suero.